2018年12月号ではPRRS対策に関する都市伝説について、科学的根拠に基づいて解明しました。今回は主にPRRSワクチンに関することを解説します。
PRRS2019.06.182018.12 養豚界
解明!PRRSワクチン都市伝説-②
スワイン・エクステンション&コンサルティング 大竹 聡 先生


はじめに
日本で豚繁殖・呼吸障害症候群(PRRS)ワクチンについて議論するたびに、国際標準から大きくかけ離れた、科学的根拠を全く伴わない持論と我流の理論がまかり通る、いわば“都市伝説” が飛び交う状況に遭遇します。前回はそのいくつかについて、真偽を科学的根拠に基づいて解明しました。本稿はその第2弾です。PRRS対策におけるPRRSワクチンの位置付けを、業界全員が正しく理解する一助となれば幸いです。
何事も「結果」がすべて。PRRS生ワクチンの子豚接種も例外ではありません。では、この場合の結果とは何でしょうか? 抗体価が上がること? 血中、ふん中、臓器中のウイルス量が減ること? いいえ、違います。PRRS対策における結果とは、あなたの農場の生産成績が改善することです。あなたは、抗体価を上げるためやウイルス量を減らすために、お金を払ってPRRS生ワクチンを使っているのですか? これも違います。あなたがお金を払ってまでPRRS生ワクチンを使っている理由は、農場の生産成績を改善させ、利益に還元させるためです。抗体価を上げたり(下げたり)、血中、ふん中、臓器中のウイルス量を減らしたりすることで、あなたの農場がもうかるわけではありません。何が本質で、それを表している指標は何なのか? これをわれわれ生産者や獣医師がしっかり理解し、判断しなければなりません。
PRRSワクチンの子豚接種を評価するための生産指標とは、すなわち①離乳〜肥育事故率②日平均増体量③出荷日齢・体重④飼料要求率です。これらの生産指標の改善が確認されて初めて、検査結果は意味を持ちます。検査結果はあくまでも参考情報に過ぎず、それのみでPRRS生ワクチンの効果を断定することはできません。
ちなみに、PRRSの検査で分かること、分からないことを以下にまとめます。
抗体検査(ELISA*)
- その個体がPRRSウイルスに感染している(もしくは過去に感染履歴がある)ことが分かります。ただ、分かるのはそれだけです。個体単位ではなく群単位で抗体価のバラツキ度合いから、その群内における感染の広がりの程度を推測することはできます
- その個体がウイルスを排せつしているか、防御免疫が発動しているか、臨床症状の強弱などは、抗体価だけでは判断できません
- ワクチン抗体と野外感染抗体の識別はできません
- ELISAで検出できる抗体は、必ずしも防御抗体(中和抗体)とは限りません
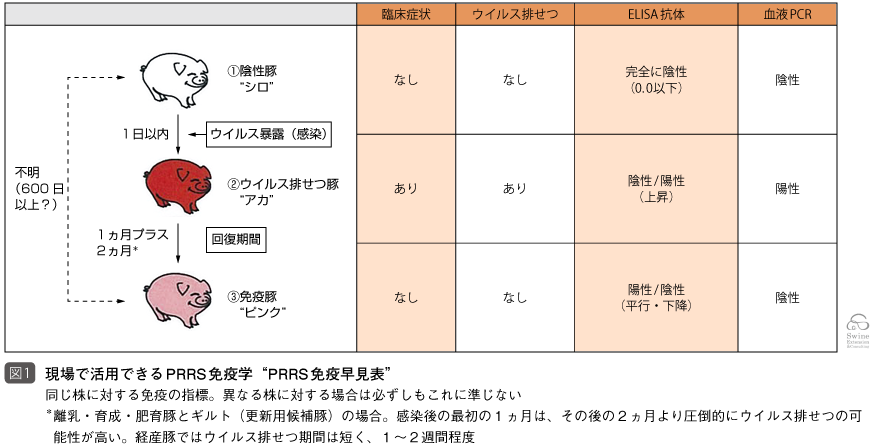
ウイルス検査(PCR)(図1)
- その個体がウイルス血症を起こしているかが分かります
- ウイルス血症を起こすのはほとんどが感染初期(感染後1〜30日くらい)なので、その個体(群)は比較的感染して間もないことが推察できます。ただ、なかには60〜90日以上ウイルス血症が持続する個体もいますので、結果の解釈には注意が必要です
- PRRSの場合、ウイルス血症と臨床症状に強い相関があることが分かっています。PCR陽性の群は、臨床症状を示している可能性が高いと推測できます。ただし、断定はできません
- PRRSの場合、ウイルス血症とウイルス排せつに強い相関があることが分かっています。PCR陽性の群は、ウイルスを排せつしている可能性が高いと推測できます。しかしながら、これも断定はできません
- PRRSの場合、防御免疫を獲得した個体(群)はウイルス血症が解消されるので、PCR陰性となります。ただし、感染していない個体も当然ウイルス血症を起こしていませんから、PCRだけでは同じく陰性の結果となります。つまり、PCRのみでは「感染が成立して防御免疫を獲得した個体」と「感染していない個体」の識別ができないのです。この課題は、ELISAによる抗体検査の併用で容易に解決できます。防御免疫が成立している個体であれば、抗体陽性(またはS/P比が0.4未満でも、小数点第1位台で何らかの数値が出ている程度の陰性)と出ますし、感染していない個体であれば、抗体価はほぼゼロになるでしょう
これは前回も触れているので繰り返しになるところもありますが、重要なので改めて解説します。PRRSウイルスがPCRにより検出された場合、そのウイルス株を同定するため遺伝子配列を読み取るシークエンス検査を行うことがあります。しかし、どれくらい一致するかという遺伝子配列の相同性(%)は、実際の防御免疫の指標にはなり得ません。シークエンス検査の結果とワクチンによる交差免疫の程度は一致しないのです。
それを証明する学術文献や現場検証試験の結果が、学会や学術誌などで多く発表されています。従って、シークエンス検査の結果は、ワクチンを使うか否かを判断する基準にはなりません。ましてや、シークエンス検査の結果から「自農場既存の野外株は、ワクチンAの株よりもワクチンBの株の方が相同性(%)が高い。だから、ワクチンBの方を使った方がよい(効果がある)」などというロジックは成立しません。
では、シークエンス検査の結果から分かることは何だったでしょうか? シークエンス検査の結果を、われわれはどのように解釈し、活用すべきだったしょうか? それは、バイオセキュリティの改善に他なりません。
シークエンス検査からは「それが野外株かワクチン株か?」「野外株であれば、どの野外株と遺伝子的に近縁か?」が分かるだけです。例えば、ずっと安定していたPRRS陽性農場でPRRSブレイクが起きたとき、ブレイク中に検出されたウイルスをシークエンス検査して、もし農場既存の株と相同性が高い株であれば、それはその既存株が何らかの要因でぶり返したと診断できます。その場合は、豚群の免疫付与や農場“内”バイオセキュリティの強化を実施します。逆に、既存株と相同性の低い株であれば、それは既存株とは全く別の株であると判断します。つまり、外部から新たに別のPRRSウイルス株が侵入したことを意味します。その場合は、外部からの侵入を許してしまったので「農場“外” バイオセキュリティのどこかに不備がなかったか?」と考え、見直しと改善を図らなければなりません。
PRRSに関しては、不活化ワクチンに比べて生ワクチンの方が効果的であることは世界標準の常識です。理由は単純明快。PRRSの防御免疫の主役は液性免疫(抗体による免疫)ではなく、細胞性免疫(抗体によらない免疫)が担っているからです。そして、PRRSの防御免疫発動に関わるマスト・アイテムが「自己細胞内で生きたウイルスが増殖すること」なのです。それがシグナルとなって、PRRS防御免疫は初めて発動します。
これは実は、豚流行性下痢(PED)やローソニア イントラセルラリスが引き起こす豚増殖性腸炎(PPE)にも当てはまり、免疫学的・ウイルス学的に証明されている、確固たる真実です。PRRSの不活化ワクチンでは、細胞性免疫を発動させるプロセスは十分ではありません。
アメリカのみならず、日本においてもPRRS生ワクチンの子豚接種の普及率は上がってきています。はるか昔「子豚接種は全然効かない……」と言われた時代が確かにありました。それもそのはず、当時はPRRS自体の病態が解明されておらず、例えば現在のPRRS対策の常識となっている「まずは母豚群の免疫安定化ありき!」ということすら、 現場では認識されていなかったのです。母豚群の免疫安定化が不十分で、母子垂直感染が存在する状況下では、PRRS生ワクチンを子豚に接種しても効果が出るわけがありません。本来ならば火を見るほど明らかな常識ですが、今になってやっとその常識が日本でも普及してきたのでしょう。
もう1つ、PRRS生ワクチンの子豚接種が普及している理由があります。それは「地域ぐるみでのPRRS対策」の価値が高まったことです。地域ぐるみのPRRS対策では、その地域内(空間レベル)での総ウイルス量低減が必要不可欠となります。バイオセキュリティの徹底だけでは、どうしても限界があるからです。
そう考えたとき、その地域内に最もウイルス排せつをしているのは、母豚群ではなく肥育豚群なのです。その肥育豚群にワクチンで免疫付与をして、ウイルス排せつを有意に抑えることができれば、その地域内における総ウイルス量を限りなく低く抑えられるでしょう。そのような有利な環境を構築できれば、地域ぐるみのコントロールや清浄化も可能なはずです。事実、日本でもそのコンセプトに基づいた成功事例が報告されています。
理由1 PRRS免疫学と現場検証の進歩
- まずは母豚群の免疫安定化が必須条件
- ワクチン接種から最低4週間は野外感染があってはならない
理由2 “地域ぐるみ” でPRRSをコントロールするコンセプト
- その地域全体のウイルス量を低減したい
- 農場密集地帯は、肥育農場で構成されているケースがほとんど
- PRRS生ワクチンは、ウイルス排せつ量を有意に低減できる

おわりに
本稿では、PRRSワクチンに関する都市伝説の真偽を明確に説明しました。
何が正しくて、何が正しくないのか? 科学的根拠を伴っているか? その最終判断をして情報を選択するのは、われわれ生産者や獣医師、つまり情報の“エンド・ユーザー” に他なりません。エンド・ユーザーであるわれわれがまずしっかりと勉強し、偏見や固定観念にとらわれることなく、最終的に自分自身で考えて正しい情報を活用することが、PRRS対策の最初の一歩なのです。

<参考文献>
- Park C et al. Vet Microbiol 172:432-442. 2014
- Park C et al. Vet Microbiol 177:87-94. 2015
- Mateu E et al. Vet J 177:345-351. 2008
- Wang L et al. Int J Vac & Im Sys 3:1-5. 2018
- 村山修吾ら.豚病会報 73:1-6. 2019
- 村山修吾.養豚界4月号:26-29. 2019



