ウイルスの検出が難しく、日本では対策が後回しにされてきた豚インフルエンザ。しかし、最新の調査で国内にも広く浸潤していることが分かり、生産性・公衆衛生への悪影響が懸念されています。流行期を前に、現場では何ができるのでしょうか。本稿では、豚インフルエンザの重要性と対策を紹介します。
なぜ今、豚インフルエンザなのか?
豚インフルエンザウイルスは、古くから豚呼吸器複合病(PRDC)を引き起こす病原体の一つとされてきましたが、豚繁殖・呼吸障害症候群ウイルス(PRRSV)、サーコウイルス2型(PCV2)、マイコプラズマ・ハイオニューモニエ(M.hp)、アクチノバシラス・プルロニューモニエ(A.pp) といった他の病原体と比べ、国内における認知度は低いのが現状です。実は近年まで、欧米においても、豚インフルエンザの養豚生産に与える影響は過小評価されていました。
転機となったのは、2009年のインフルエンザパンデミックの発生でした。パンデミック発生直後のウイルス遺伝子の解析により、その原因ウイルスが、それまで北米とヨーロッパでおのおの流行していた2種類の豚インフルエンザウイルスの遺伝子を併せ持つことが判明したため、豚インフルエンザの公衆衛生における重要性がクローズアップされました。
またパンデミックの発生からほどなくして、ヒトから豚へのパンデミックウイルスの感染が世界各地で相次いで報告され、特に北米の養豚生産現場では明瞭な被害(呼吸器疾病の増加や生産性の低下)が認められたことから、畜産衛生における影響も慎重に評価する必要性が生じました。そこで、欧米諸国を中心に、公衆衛生と畜産衛生の各担当部局が足並みをそろえながら、豚インフルエンザの大規模なサーベイランスが進められました。 その結果、各国の養豚場において豚インフルエンザウイルスが広くまん延し、PRDCの発生要因として大きな役割を担っていることが明らかになってきました。
国内における豚インフルエンザサーベイランス体制は未整備ですが、後述するわれわれの研究結果から、国内養豚における豚インフルエンザウイルスの全国的な流行も確認されているので、海外と同様の影響をもたらしていると推察されます。
見えにくい豚インフルエンザの影響
これまで養豚業界において豚インフルエンザが軽視されてきた要因は、いくつか考えられます。豚インフルエンザは食欲不振や発咳・発熱など急性の呼吸器症状を引き起こしますが、他の病原体と複合感染を起こさない限り、重症化することはほとんどありません。また、豚インフルエンザウイルスは呼吸器官で限局的に感染・増殖し、ウイルス血症は起こしません。発症豚からのウイルス排せつ期間も短く、初感染の若齢豚であっても1週間程度で体内から完全にウイルスが排除されます。
さらに、ウイルスが盛んに増殖する日齢も限られていて、母豚から質・量ともに十分な移行抗体が得られなかった哺乳子豚や、移行抗体の効力が消失する90日齢以降の肥育豚が初感染した場合を除くと、高感度な遺伝子検査を用いてもウイルスを検出するのは困難です。つまり、農場内における豚インフルエンザウイルスの存在を直接確認するには、検査対象日齢を絞って繰り返し鼻腔スワブを検査する必要があります。
一つ、ウイルス血症を起こすPRRSVやPCV2、あるいは持続感染するM.hpやA.ppといった他の病原体は、比較的容易に検出することができます。その結果、実際には豚インフルエンザウイルスが生産性低下の主因となっているケースでも、上記のような病原体が“濡れ衣を着せられる” ことになります。
豚インフルエンザの検査法
豚インフルエンザを含め、あらゆる感染症の検査法は大きく2種類に大別できます。一つは「病原体の存在を確認する検査」で、病原体を構成する遺伝子やタンパク質の検出、感染性を備えた病原体の分離が該当します。検査に適した検体は、検査対象とする病原体ごとに異なり、豚インフルエンザの場合、前述のように採材部位や日齢に大きな制約があります。 一般に、遺伝子やタンパク質の検出は迅速かつ簡便ですが、例え検査結果が陽性でも「生きた(感染性を備えた)病原体」がいるとは限らないので、その存在を確定するためには病原体の分離が必須です。
もう一つは「病原体の感染歴を確認する検査」で、血液検体を用いて、病原体と反応する抗体を検出します。一口に「病原体と反応する抗体」と言っても、生体内では性質の異なるさまざまな抗体が生産されていて、一般的な抗体検査法(ELISA法など)で検出されるのは「病原体を構成するタンパク質のどこかに反応するあらゆる抗体」です。
これに対して、主にウイルス感染症の検査で実施される中和試験では、「病原体の細胞への接着・感染を阻害する(中和活性を示す)抗体」のみが選択的に検出されます。中和試験の場合、抗体と反応させる病原体(抗原)の種類が検査結果を大きく左右するため、豚インフルエンザウイルスのように表面タンパク質が盛んに変異する病原体を対象とした検査では、農場内での流行が疑われる株と近縁な抗原を使用する必要があります。
ちなみに、豚インフルエンザの抗体検査で盛んに実施されるHI試験(赤血球凝集阻止試験)は、中和試験の代替法と位置付けられます。また若齢豚の抗体検査では、母豚からの移行抗体の影響を考慮する必要があります。移行抗体が検出される日齢の限界は、対象病原体や検出法によって前後することが知られていますが、豚インフルエンザウイルスの場合、中和活性を示す移行抗体は70日齢程度まで検出されます。
日本にも広く浸潤─わずか4年で全国に拡大か
豚インフルエンザウイルスは、ウイルス粒子表面のヘマグルチニン(HA)というタンパク質を介して細胞に接着することで感染します。そのため、HAに反応する抗体は中和活性を示します。HAの構造はバリエーションが豊富で、抗体との反応性(抗原性)の違いによって、亜型と呼ばれるグループに分類されます。現在世界中の養豚現場で流行しているウイルスのHA亜型は、H1亜型とH3亜型の2種類ですが、実際には同じHA亜型のウイルス株の間でも、相当程度の抗原性の違いが認められます。例えば、90年代初頭から国内養豚での流行が確認されている古典的なウイルスと2009年のパンデミックウイルス(pdm2009ウイルス)はいずれもH1亜型ですが、その抗原性は明確に違います。
われわれは、国内養豚場における豚インフルエンザの流行状況を明らかにするため、全国27道県179農場から母豚1,598頭分の血清(2013年採血)を集め、近年国内で分離された4株の豚インフルエンザウイルス株(H1亜型とH3亜型を各2株)を基に調整したウイルス抗原を用いて、中和試験を実施しました。検査対象を母豚に絞った理由は、肥育豚に比べて飼養期間が長いためウイルスに感染する機会が多く、各農場におけるウイルス流行状況の的確な把握に適しているからです。その結果、27道県(100%)、174農場(97.2%)、1,417頭(89.0 %) の血清から、試験に用いたいずれかのウイルス抗原に対する中和抗体が検出されました。また4種類のウイルス抗原のうち、pdm2009ウイルスを基にしたものが最も高い陽性率(86.0%)を示しました(表1)。
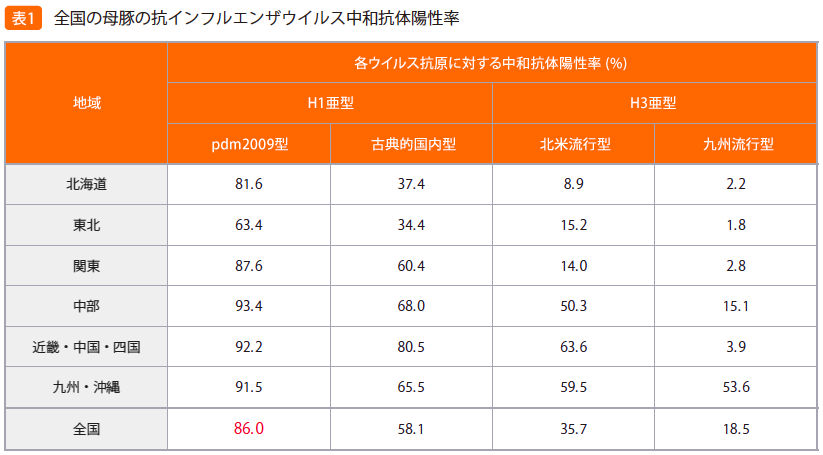
- 全国27道県179農場の母豚1, 598頭分の血清を検体として、抗原性の異なる4種類のウイルス抗原(H1亜型pdm2009型、H1亜型古典的国内型、H3亜型北米流行型、H3亜型九州流行型)に反応する抗体の有無を中和試験により調べた
- H1亜型pdm2009型ウイルスの全国的な浸潤の他、H3亜型北米流行型ウイルスの西日本における流行、H3亜型九州流行型ウイルスの九州を中心とした限局的な流行が示唆された
さらにわれわれは、豚インフルエンザウイルスの分離とその遺伝的性状の解析にも取り組んでいます。豚インフルエンザウイルスの遺伝子は8本に分節化していて、各遺伝子分節が個別に変異・進化することが知られていますが、2013年以降に全国10農場から分離された26株のウイルス遺伝子を解析した結果、pdm2009ウイルスに由来する遺伝子分節が幅広く共有されていることが分かりました(表2)。これらの結果はpdm2009ウイルスが、その出現からわずか4年程度で全国の養豚場にまん延したことを示唆しています。
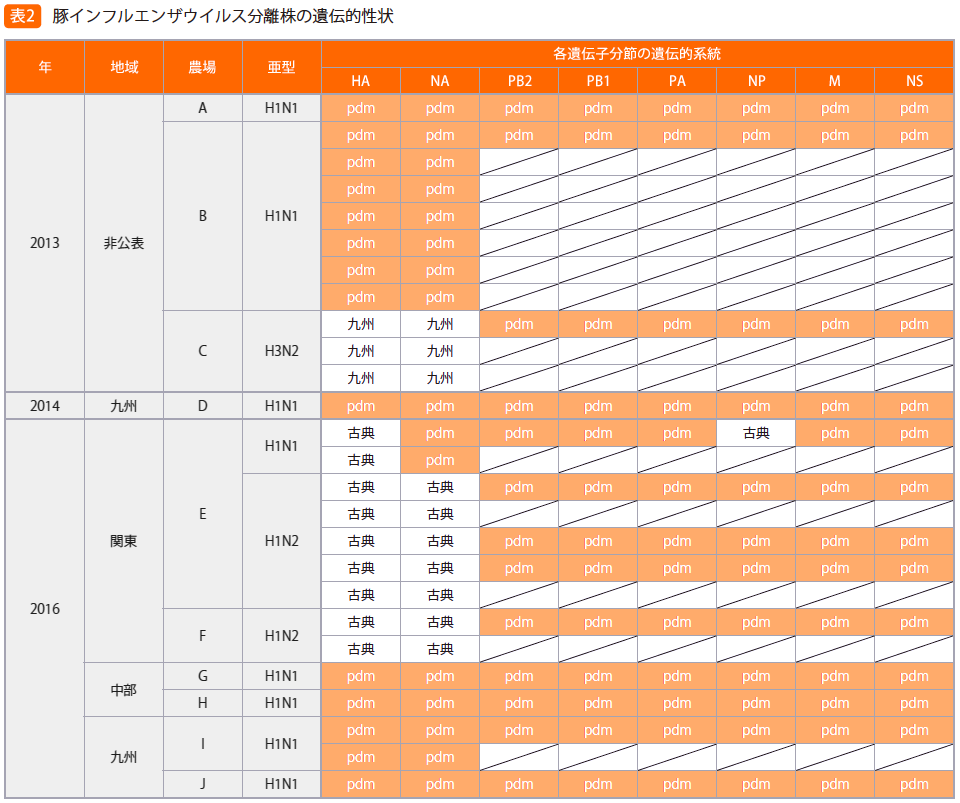
- 全国10農場の養豚から分離された26株の豚インフルエンザウイルスのHAおよびNA遺伝子分節と、各農場の代表株の内部遺伝子分節(HAおよびNA遺伝子分節以外の6遺伝子分節)の遺伝子を解析し、各遺伝子分節の遺伝的系統を調べた
- pdm:H1亜型pdm2009型、九州:H3亜型九州流行型、古典:H1亜型古典的国内型、H3亜型北米流行型
対策のポイント
ウイルス全般に共通する性質として、①生きた動物・細胞の中でのみ増殖する②乾燥に弱いという2点を理解する必要があります。
例えば多くの細菌は、豚舎の隅っこや水たまりでも、十分な栄養素があればどんどん自己増殖していきます。しかし生きた細胞が分裂・増殖する仕組みを巧みに利用しながら増殖するウイルスは、環境中に感染性を維持したまま潜むことはあっても、そこで勝手に増えることはありません。
また、ヒトのインフルエンザをはじめ多くの呼吸器感染症が冬季に流行することから、「ウイルスは乾燥に強い」との認識が広がっているようですが、これは完全に誤解です。生体の呼吸器表面は粘性のある液体成分で覆われ、病原体の侵入から保護されていますが、乾燥期にはこの粘液層が薄くなるため、病原体が呼吸器まで到達・侵入するリスクが上昇します。言い換えるなら「生体が乾燥に弱い」のです。そしてウイルスも実際、乾燥環境下に置かれると速やかに失活し、その感染性を失います。
ここからいえる効果的なウイルス対策は、「空舎期間の設定」と「豚舎の洗浄と乾燥」です。オールイン・オールアウトも有効な手段ですが、矢継ぎ早に次のロットが搬入されている場合、十分な効果は期待できません。また空舎期間をどれだけ長くとっても、内部が汚れている、あるいは湿っているようでは、環境中のウイルスは死滅しません。短期間でも構わないので、豚舎内を乾燥させることが重要です。
豚インフルエンザウイルスの遺伝子を解析すると、その祖先のほとんどがヒトの流行株だと分かります。つまり、従業員の方から農場の豚へ感染したウイルスが、いつしか豚の間で流行しているわけです。とりわけ、pdm2009ウイルスのような新しいウイルスが各農場へ侵入する際、このヒト→豚感染ルートは決定的な役割を担っています。
インフルエンザ感染が疑われる従業員の方に作業を控えていただくのはもちろんですが、従業員、さらにはその家族の方々も含めて、皆さんでインフルエンザワクチンを投与することにより、ヒト→豚感染リスクを抑えることが可能です。
より積極的な豚インフルエンザ対策として、強制馴致*やワクチン投与が挙げられます。ただし豚インフルエンザの場合、前述のようにウイルスの増殖部位も排せつ期間も限られているので、十分な馴致材料を確保するのはほぼ不可能です。
豚インフルエンザワクチンは、現在2社から不活化ワクチン(2回投与)が発売されています。どちらも子豚用のワクチンで、移行抗体の影響を考慮すると、6週齢から10週齢の間に2回投与することで最大の効果が得られると考えられます。一方、母豚へのワクチン投与は、前述のように国内養豚場のほとんどの母豚が豚インフルエンザの感染を経験していることもあり、その効果は限定的な場合が多いようです。
*獣医師の指導の下で行ってください。
おわりに
哺乳〜離乳期のPRDCに困っている農場は、とても多いと思います。そしてその大半が、一般的な検査で検出される主要な病原体に対して、すでに具体的な対策(ワクチンや抗菌薬)を施しているものの、十分な効果が得られず頭を抱えているはずです。もしまだ今回紹介したような豚インフルエンザ対策を実践されていないようであれば、ウイルスや抗体の検査を含め、試す価値は十分にあると思います。 また万が一、新しいパンデミックウイルスが国内養豚から発生するような事態になれば、国内養豚への甚大な風評被害も予想されます。そのリスクを低減するためにも、ぜひ豚インフルエンザ対策をご検討いただければと思います。







