はじめに
牛呼吸器病症候群(BRDC)はウイルスや細菌などの病原微生物がストレスや飼養環境下において複雑に絡み合い呼吸器病発症に至る疾病である1)。BRDCは病原微生物として牛RSウイルス、牛パラインフルエンザウイルス3型、牛伝染性鼻気管炎ウイルスなどのウイルスおよびMycoplasma bovisなどが一次的に感染あるいは存在し、その後、Mannheimia haemolyticaが感染すると一層、重篤化する。また、Pasteurella multocidaなどの日和見的な細菌が感染することが常である2)。BRDCの発症に伴う治療としては、主に細菌感染をターゲットとして抗菌剤が使用されるが、その選択にあたっては、起因菌に対する抗菌活性(最小発育阻止濃度〈MIC〉など)を考慮するだけではなく、実際に投与した後の体内分布・代謝といった薬物動態も併せて考慮する必要がある3)。
近年、興味深い薬物動態を示す長期持続型抗菌剤がBRDC治療に広く応用されるようになった。例えば、新しいマクロライド系抗菌剤であるツラスロマイシンは肺組織への移行性がきわめて良好であり、肺における半減期は184時間という薬物動態を示す4)。一方、セファロスポリン系の抗菌剤であるセフチオフルの持続型製剤においては、徐放作用を応用することにより有効濃度を持続させることに成功している5)。マクロライド系やセファロスポリン系の抗菌剤は一般的に時間依存性であることから、有効濃度を一定期間持続させるこれらの剤型は臨床的により有効性を発揮させることが可能となる。
本稿では、これら持続型抗菌剤を応用する際の課題や、一定の治療後経過観察期間(Post Treatment Interval:PTI)を取り入れた新しい考え方に基づく治療方法について紹介する。
持続型抗菌剤の利点や懸念とは
一般的に、時間依存性の抗菌剤では、ターゲットとする器官や組織においてMIC以上の治療有効濃度をどの程度維持・持続できるかが有効性の決め手となる。
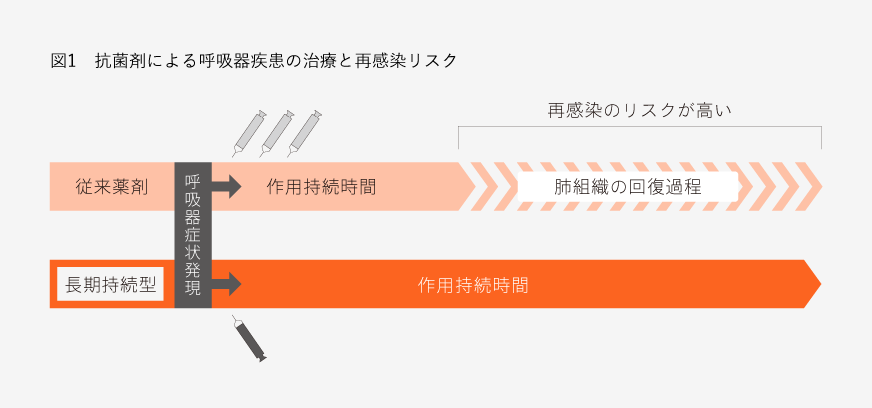
ここで有効濃度を持続させることの意味を考えてみたい。有効濃度を維持すべき期間とは、抗菌剤が病原菌を増殖できなくさせ、最終的に死滅させるのに必要な期間であることはもちろんだが、その後の組織の修復期間にも目を向ける必要がある。BRDCを発症した牛では気管支炎や肺炎により組織が障害を受けている。抗菌剤により病原菌を一掃した後も、障害を受けた組織が修復されるまでには1週間からそれ以上の時間がかかり6)、その期間は再感染に対する免疫機能が制限されるため、十分なケアが必要である。人間であれば風邪を引いた際には清浄な環境下で十分療養できるが、牛ではたとえ病畜ペンに移動させたとしても、常に病原体の侵入や攻撃に曝されることになる。しかし持続型抗菌剤を使用すれば、病原菌を一掃した後の「再感染高リスク期間」である組織修復に要する期間も抗菌作用により防護される。このため、速やかな回復と再発の低減に持続型抗菌剤は有利に働くと考えられる(図1)。
一方、持続型抗菌剤を使用するに際しての懸念点として、薬剤耐性の発現と抗菌剤の使用量増加が挙げられる。まず、薬剤耐性の発現を抑制するには、薬物動態学/薬力学(PK/PD)パラメーターに基づく使用が求められており7)、時間依存性の持続型抗菌剤においては、1回の投与で一定期間、標的組織においてMIC以上の濃度を維持し、十分な抗菌作用を発揮するため、耐性菌発現の低減が期待できる。加えて、各薬剤の特徴も十分な抗菌作用を発揮するうえで有利に働く。気管支や肺で炎症が起こると食細胞が動員されるのが常だが、ツラスロマイシンは好中球やマクロファージなどの食細胞内に高濃度に蓄積される特徴がある8)ことから、炎症部位において食細胞内に蓄積されていたツラスロマイシンが放出され、より高濃度かつ長期間にわたり有効濃度が持続する。また、M. haemolyticaやP. multocidaに対するツラスロマイシンのMICと最小殺菌濃度(MBC)は70%の菌株で一致しており4)、これらの菌に対してはほぼ殺菌的に働くことも薬剤耐性の発現低減に寄与するものと考えられる。一方、セフチオフルの体内動態の特徴として、投与後にデスフロイルセフチオフルに変換され、血漿タンパク質と可逆的に結合し、より高濃度に炎症部位に移行することが挙げられる9)。実際に、近年の薬剤感受性試験成績においてもセフチオフルに対する肺炎起因菌の耐性化傾向は認められていない10、11)。以上のことから、PK/PDパラメーターに基づく投与による確実な抗菌作用によって薬剤耐性の発現を低減できると考えられる。
抗菌剤は、国が策定した「薬剤耐性対策アクションプラン」12)で示されているとおり、慎重使用が求められ、動物用医薬品検査所などが実施している家畜由来細菌の薬剤耐性モニタリング(JVARM)によって、使用量(販売量)がモニタリングされている。呼吸器病の治療の際に必要な抗菌剤の量としては、一般的な抗菌剤では複数回の投与が必要であることから総量(総力価)が多くなるが、持続型抗菌剤の投与回数は1回であり、治療に使用する抗菌剤の総力価としては低減すると考えられる。さらに、持続型抗菌剤は呼吸器病の再発を軽減できることも報告されている13)。
治療後経過観察期間「Post Treatment Interval(PTI)」
抗菌剤を使用した後、病畜の症状が改善しない(呼吸状態が改善しない、解熱しない、鼻汁が漏出しているなど)ため、再治療を行うケースは多いと思われる。ここで、抗菌剤の使用と臨床症状との関係を改めて考えてみたい。
抗菌剤としての役割はあくまで細菌を増殖させないようにし、最終的に死滅させることであり、症状の改善には牛自体の免疫機能や組織修復力が関わっている。つまり、抗菌剤が作用し病原菌が死滅していても、何らかの臨床症状を呈している場合は、過度の炎症が継続している場合や組織修復が行われている最中であるということである。つまり、抗菌剤としての作用が持続しているのであれば、症状が残っていたとしても抗菌剤で再治療をする必要はないということである。米国では持続型抗菌剤を利用できるようになってから、治療後経過観察期間(Post Treatment Interval:PTI)という考え方を取り入れた治療方法が提案されている。PTIとは、「有効濃度が維持されている期間は症状があっても様子見として積極的な追加治療を行わない」という考え方である14)。この背景には、持続型抗菌剤の有効濃度を維持している期間に行う追加治療が無駄になるということだけではなく、再治療のために牛を捕獲し、保定を行うことが牛にとってストレスになるため、安静にしておく方が良いのではないか、という考えが存在する。病原菌を排除した後に炎症が治まり、組織修復が行われていく過程で徐々に臨床症状も改善していくものと考えられる(図2)。日本では馴染みのない考え方ではあるが、その効果はどのようなものだろうか。ここでは、米国において実施されたPTIの有効性確認試験を紹介する。
試験1
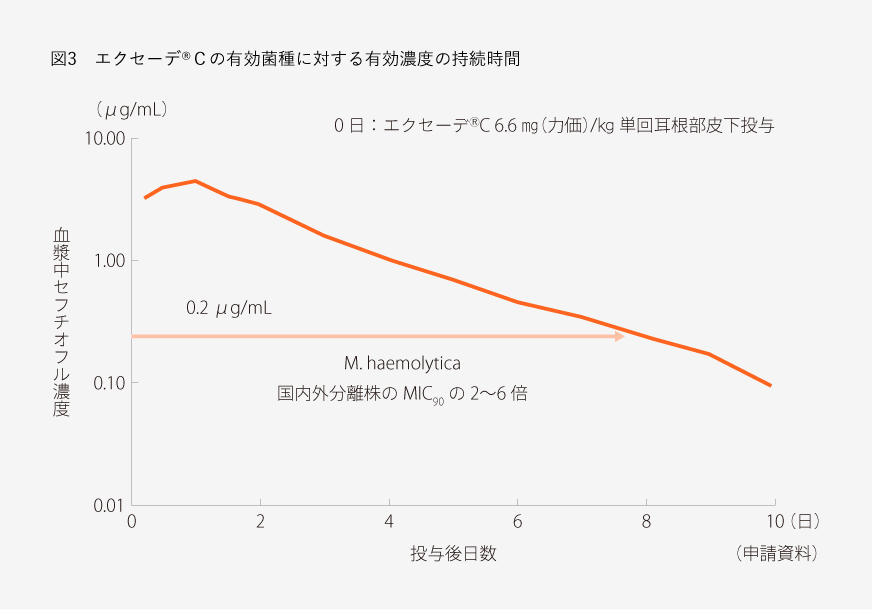
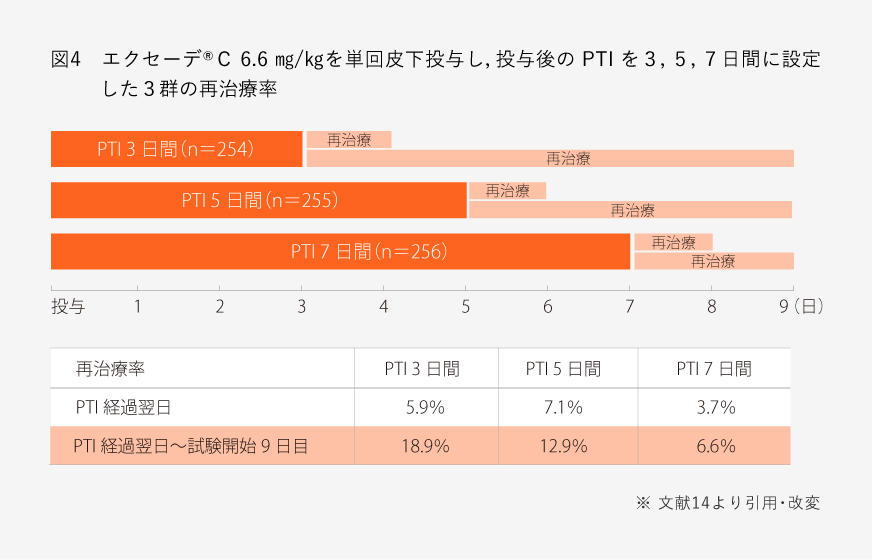
米国のフィードロットにおいて、肺炎罹患牛に対してエクセーデ®C6.6㎎/㎏を単回皮下投与し、投与後のPTIを3、5、7日間に設定した3群に分けた。最長のPTIを7日間に設定したのは、エクセーデ®Cの有効菌種に対する有効濃度の持続時間が少なくとも7日間であることに基づいている(図3)。まず、PTI終了翌日における再治療率を比較したところ、各PTI群間に差は認められなかった。つまり、治療後7日間のPTIを設定しても、PTI3日間や5日間の群に比べて再治療を必要とする頭数が増えることはなかった。さらに、PTI経過翌日から試験開始9日目までの再治療率を比較したところ、PTI7日間の群は他群に比べて有意に低かった。つまり、PTI3日間または5日間の群において実施された再治療は、有効濃度を維持している間に行われたものであり、症状は認められるものの回復に向かっている牛に行われたもので、結果的に不必要な治療であったことが示唆された14)(図4)。
試験2
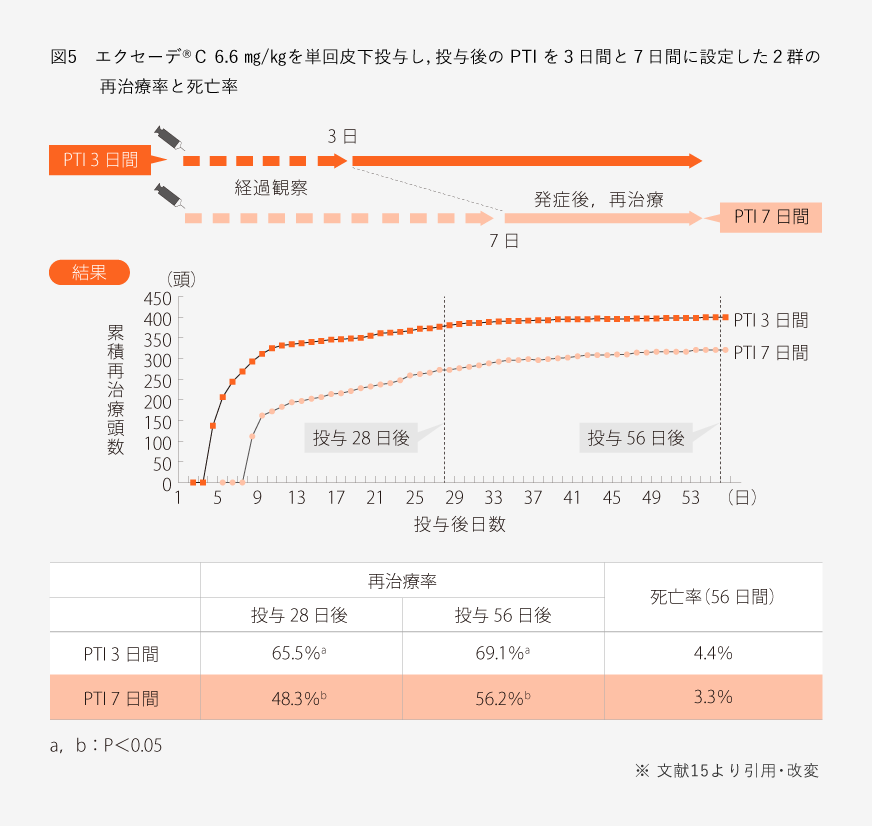
米国のフィードロットにおいて、導入後に肺炎に罹患した肥育牛に対してエクセーデ®C6.6㎎/㎏を単回皮下投与し、ランダムにPTI3日間または7日間の群に割り付けた。それぞれのPTI終了後、呼吸器症状および活力減退の症状を呈した牛に対して再治療を実施した。この両群において再治療頭数、再治療率および死亡率を比較した結果、PTI7日間の群で投与28日後および投与56日後の再治療率が有意に減少し、一方、死亡率には両群で有意差はなかった(図5)。つまり、PTIを7日間と設定しても肺炎が重症化して死亡頭数が増えることはなく、再治療頭数を削減できたことを示している15)。
試験1および2の結果から、適切なPTI期間の設定により不必要な治療を削減できただけでなく、回復に要する期間をケアし、より良い環境下で飼育可能とすることによりPTI期間が終了した後の長期にわたり再発牛を削減できたものと推察できる。
PTIのメリットと実践
上記試験の結果から、PTIを設定することにより不必要な再治療を削減できることが示唆された。これにより労働コストや治療コストをも削減でき、さらには抗菌剤の使用量も削減できるため、呼吸器病起因菌の薬剤耐性獲得機会を最小化できる可能性がある(図6)。 米国でPTIを取り入れた治療が実践されている背景の1つは、農場規模が大きく、1頭当たりにかけられる労力・時間が限られていることである。大規模なフィードロットにおいて病畜を発見し、捕獲して保定するという作業は多大な労力を要し、また病畜へ大きなストレスを与えるため、治療の機会、すなわち捕獲の機会は可能な限り少なくする必要がある14、15)。
一方、日本でPTIを取り入れた治療を実践する際には、米国とは飼養管理方法が異なること、また牛1頭当たりの経済的価値も異なることを考慮し、工夫して実施する必要がある。PTIを初めて実践する際には、再治療を行わない経過観察期間を設定することに対して畜主が不安を覚えることがあるだろう。そのため、当初設定するPTIはその薬剤が有効濃度を維持する最長の期間ではなく、短い期間からはじめることが良いのではないか。例えば、一般的な抗菌剤の投与は3日間を1クールとして行われることが多いため、まず3日間のPTIからスタートし、経過を確認しながらPTIを徐々に延ばしていくことで畜主の不安も和らぐのではないかと思われる。さらに、当該農場における呼吸器病の起因菌を特定し、抗菌剤に対する感受性を確認することにより、より安心して経過観察を行うことができると思われる。なお、前述の試験で用いられたエクセーデ®Cは7日間が最適なPTIであったが、他の薬剤では有効濃度の持続期間が異なるため、それぞれの薬剤に適した期間を設定する必要がある。またPTIに限ったことではないが、病畜が重篤化する前に早期発見・早期治療を行うことはもちろん重要であり、炎症・組織損傷の程度を抑え回復をより早く完全なものにすることができると考えられる。
おわりに
近年、農場の大規模化が進むなかで、1頭当たりにかけることができる時間、労力、費用は相対的に減少していくものと思われる。また、薬剤耐性菌の問題も大きくクローズアップされているなか、抗菌剤の使用量を削減する取り組みも求められている。米国の大規模農場で取り入れられているPTIという新しいコンセプトに基づく抗菌剤の使用方法は、治療に要する労力・コスト・抗菌剤使用量を削減できる可能性があり、今後我が国でも取り入れるべき手法であると思われる。
<参考文献>
- 1) Hilton WM:Anim Health Res Rev, 15(2), 120-122(2014)
- 2) Cravens RL:臨床獣医,22(6),15-19(2004)
- 3) 農林水産省:牛呼吸器病(BRDC)における抗菌剤治療ガイドブック(2018)
- 4) Evans NA:Vet Ther, 6(2), 83-95(2005)
- 5) Hibbard H, Robb EJ, Chester ST Jr, et al.:Vet Ther, 3(1),22-30(2002)
- 6) 播谷亮:家畜感染症学会誌,2(3),85-97(2013)
- 7) 勝田賢:家畜感染症学会誌,2(1),1-8(2013)
- 8) Siegel T, Earley DL, Smothers CD, et al, : J Anim Sci, 82(Suppl1), 186(2004)
- 9) Washburn K, Johnson R, Clarke CR, et al.:J Vet Pharmacol Ther,28(3), 247-251(2005)
- 10) Portis E, Lindeman C, Johansen L, et al.:J Vet Diagn Invest, 24(5), 932-944(2012)
- 11) Magstadt DR, Schuler AM, Coetzee JF, et al.:J Vet Diagn Invest,30(1), 99-104(2018)
- 12) 厚生労働省:薬剤耐性対策アクションプラン(2016)
- 13) Nautrup BP, Vlaenderen IV, Decker M, et al.:Bov Pract, 51(1),1-13(2017)
- 14) Apley MD:Vet Clin North Am Food Anim Pract, 31(3), 441-453(2015)
- 15) Meyer J, Moseley W, Lehman F, et al.:23rd World Buiatrics Congress Proceeding(2004)